 uzaklığı moleküler hızın
büyüklüğü ile orantılıdır ve tüm yönlere doğru moleküler hızların
dağılımı aynı olduğundan izotropik bir davranış gösterir.
uzaklığı moleküler hızın
büyüklüğü ile orantılıdır ve tüm yönlere doğru moleküler hızların
dağılımı aynı olduğundan izotropik bir davranış gösterir. Çeşitli hız ve enerjilere sahip moleküllerin sayısına ilişkin temel
eşitlik Boltzmann Dağılımı ile verilir. Kinetik moleküler teori temel alan modele
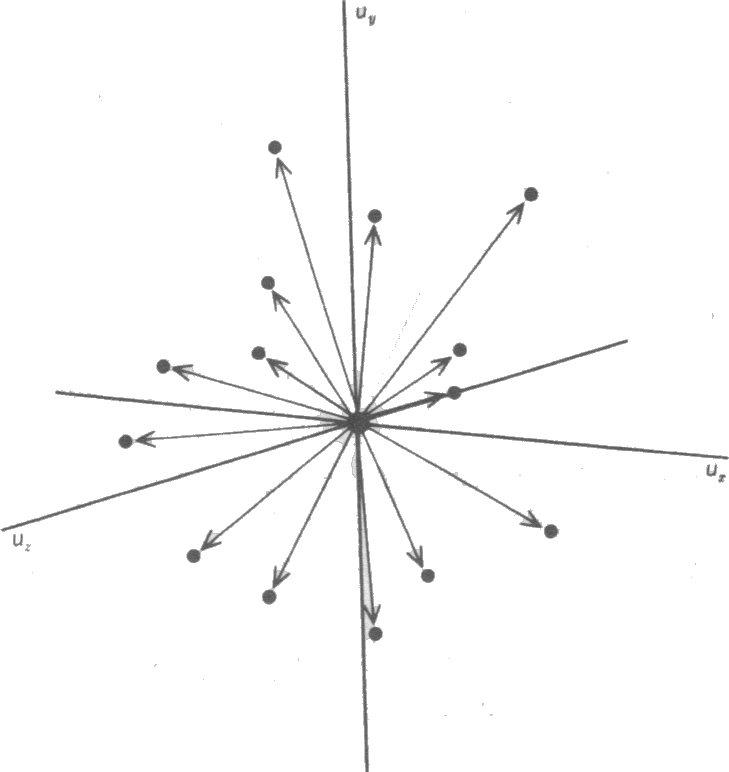
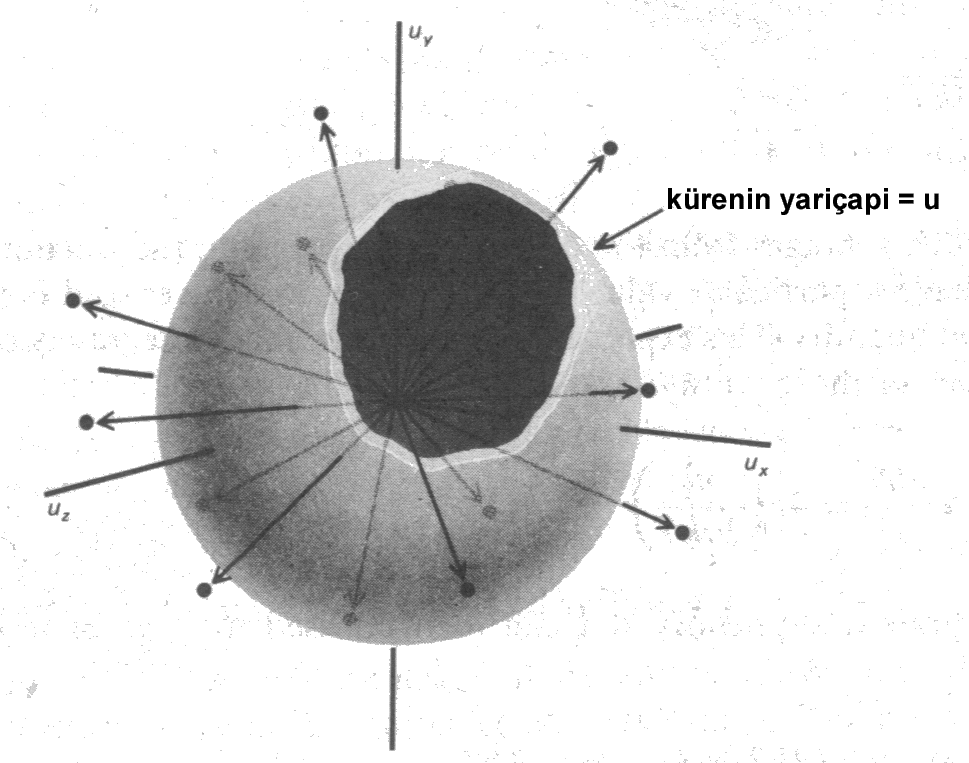
göre; gaz molekülleri çeşitli hızlarla ve çeşitli yönlere doğru hareket eder. Bu
hızlar Şekil 1 de gösterilmiştir. Şekildeki herbir noktanın orjinden  uzaklığı moleküler hızın
büyüklüğü ile orantılıdır ve tüm yönlere doğru moleküler hızların
dağılımı aynı olduğundan izotropik bir davranış gösterir.
uzaklığı moleküler hızın
büyüklüğü ile orantılıdır ve tüm yönlere doğru moleküler hızların
dağılımı aynı olduğundan izotropik bir davranış gösterir.
Özel birr yöne doğru örneğin x yönündeki hız dağılımını
araştırabiliriz. Eğer ![]() ile
ile ![]() hız aralığındaki moleküllerin dN/N kesrini
bulmalıyız. Şekilde öne doğru hareket eden moleküllerin
hız aralığındaki moleküllerin dN/N kesrini
bulmalıyız. Şekilde öne doğru hareket eden moleküllerin ![]() hız pozitifken zıt yöne hareket eden
moleküllerin hızı ise negatiftir. Bu hız aralığındaki moleküllerin kesri için;
hız pozitifken zıt yöne hareket eden
moleküllerin hızı ise negatiftir. Bu hız aralığındaki moleküllerin kesri için;
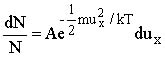
kullanılır. Buradaki A orantı sabitidir. Bu sabitin değeri, eşitliğin
sağ tarafının integralininden hareketle hesaplanabilir. ![]() hızının her iki yöndeki tüm olasılıkları
hızının her iki yöndeki tüm olasılıkları
![]() arasında yer alacaktır. Bu nedenle bu hız aralığında dN/N
değeri 1 olcaktır.
arasında yer alacaktır. Bu nedenle bu hız aralığında dN/N
değeri 1 olcaktır.
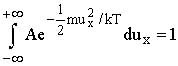
böylece hız sabiti için
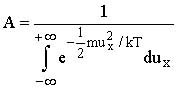
yazılabilir. Bu eşitlikten A nın değeri
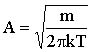
olarak hesaplanabilir. Sonuçta N molekülün x yönündeki hız dağılımına ilişkin
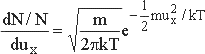
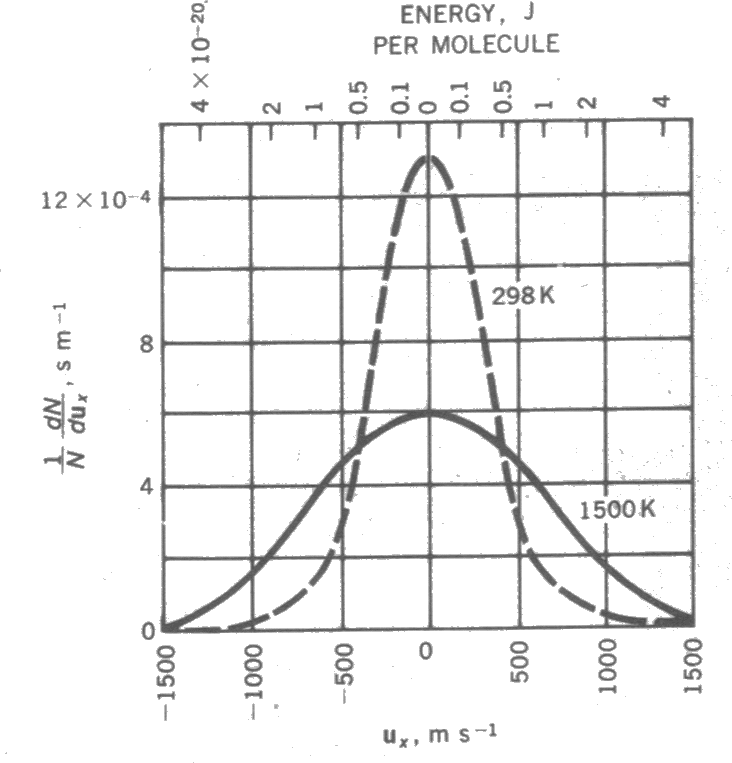
yazılabilir. Aşağıdaki şekilde azotun iki farklı sıcaklıktaki bir boyuttaki dağılımı verilmiştir.
Üç boyuttaki hız dağılımı için bir boyuttaki hız dağılımına
benzer şekilde moleküllerin x, y ve z doğrultularındaki hız kesirlerini bulabilmek
için ![]() -
- ![]() ,
, ![]() -
- ![]() ,
, ![]() -
- ![]() hız
aralığındaki molekülleri dikkate almalıyız. Bu nedenle;
hız
aralığındaki molekülleri dikkate almalıyız. Bu nedenle;
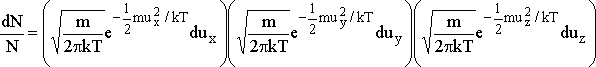
veya
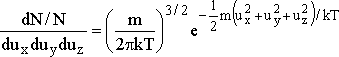
 yazılabilir. Yandaki şekildeki
gibi bir hacim elemanı içerisindeki moleküler noktaların yoğunluğunu
belirleyebiliriz. Bunlar u hızına sahip moleküllerdir. Çünkü bu küresel kabuğun
hacmi 4pu2du kadar olup bu
elementteki noktaların sayısı yukarıdaki eşitliğin 4pu2du/duxduyduz
ile çarpılmasıyla elde edilir.Burada
yazılabilir. Yandaki şekildeki
gibi bir hacim elemanı içerisindeki moleküler noktaların yoğunluğunu
belirleyebiliriz. Bunlar u hızına sahip moleküllerdir. Çünkü bu küresel kabuğun
hacmi 4pu2du kadar olup bu
elementteki noktaların sayısı yukarıdaki eşitliğin 4pu2du/duxduyduz
ile çarpılmasıyla elde edilir.Burada ![]() değişimi yapılırsa üç boyutlu
hız dağılımı için
değişimi yapılırsa üç boyutlu
hız dağılımı için
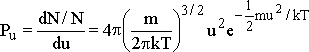
elde edilebilir.Aşağıda iki farklı sıcaklıkta N2 için Maxwell-Boltzmann dağılımı çizilmiştir.Düşük sıcaklıklarda moleküler hızlar dar bir aralıkta dağılırken, yüksek sıcaklıklarda aralık genişlemektedir. Ayrıca eğrilerin maksimum değerleri sıcaklığa bağımlı olarak değişmektedir.
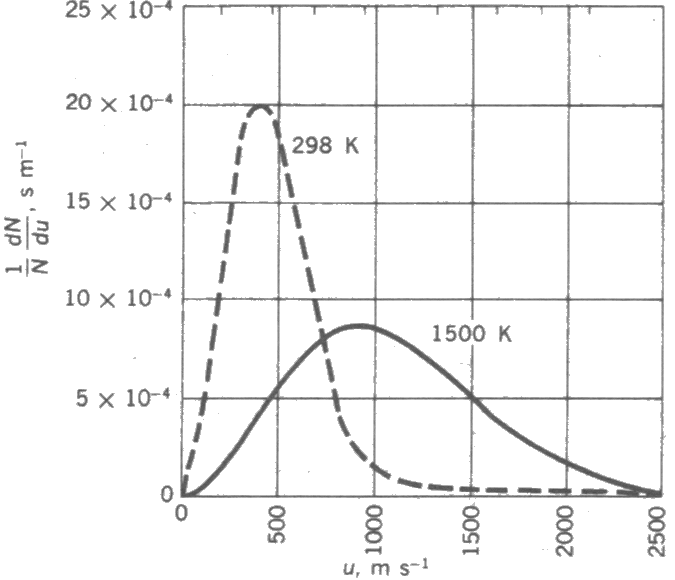
Daha önce kinetik teoriden hareketle moleküler hızların hız kareleri
ortalamalı karekökü hızının ![]() olduğunu göstermiştik. Moleküler
hız dağılım eşitliğini kullanarak ortalama moleküler hızların nasıl
değiştiğini hesaplayabiliriz. Bu amaçla;
olduğunu göstermiştik. Moleküler
hız dağılım eşitliğini kullanarak ortalama moleküler hızların nasıl
değiştiğini hesaplayabiliriz. Bu amaçla;
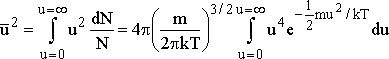
yazarsak eşitliğin integralinin sonucu
![]()
verir. Sonuç olarak kinetik moleküler teori ile uygun olan ![]() eşitlik elde edilmiş olur.
eşitlik elde edilmiş olur.
Benzer şekilde ortalama hız, ![]() , değeri de benzer yaklaşımlarla
, değeri de benzer yaklaşımlarla
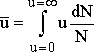
ve
![]()
şeklinde elde edilir. Bu hızlar dışında hız - olasılık grafiklerindeki maksimum olasılıklı hızı da belirleyebiliriz. Bu grafiğin maksimum değerine karşı gelir. Bunun için
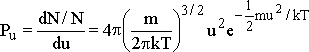
fonksiyonun dc ye göre türevini sıfır yapan c değeri hesaplanmalıdır.
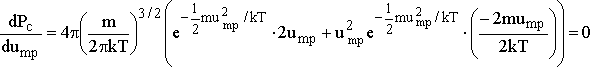
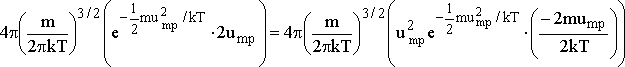
eşitliğin her iki tarafı
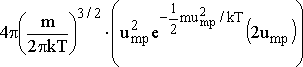
bölünürse
![]()
eşitliği elde edilir. Böylece maksimum olasılıklı hız için
![]()
bağıntısı elde edilir (1).