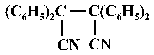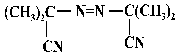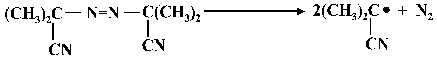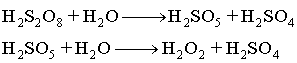Emülsiyon
Polimerizasyonu
Emülsiyon polimerizasyonu başladığı ortamdaki bileşenlerin
varlığı ve fiziksel doğalarına göre, klasik
emülsiyon polimerizasyonu, ters
emülsiyon polimerizasyonu ve emülgatörüz
emülsiyon polimerizasyonu olarak, üç grup altında incelenebilir. Klasik
emülsiyon polimerizasyonunda, reaksiyonun başında polar bir fazda monomerle birlikte emülgatör dağılmış durumdadır.
Ters emülsiyon polimerizasyonunun klasik emülsiyon polimerizasyonundan farkı;
monomerin polaritesi fazlayken dağıldığı ortamın polaritesi çok daha
düşüktür. Emülgatörsüz emülsiyon
polimerizasyonunda reaksiyon başında ortama emülsiye edici hiçbir ajan konulmaz
ve emülgatörler zamanla reaksiyon sırasında oluşur.
Emülsiyon polimerizasyonunun yürüyüş doğası ve yürüyüş şeklinin daha iyi anlaşılabilmesi için öncelikle ortamda bulunan ya da reaksiyon sırasında oluşan türlerin fiziksel doğasını anlamaktan geçer.
1.2.G.1.
Emülsiyon Polimerizasyonunda Yüzey Aktif Maddelerin Rolü
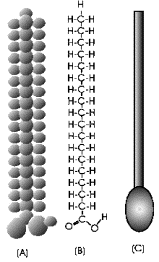
Sabun molekülleri, yağ asitleri, uzun zincirli alkoller
gibi polar bir uca ve uzun bir apolar bir kısma sahip bir molekül olup, polar
bir çözgende çözündüğünde kritik bir konsantrasyonun üzerinde miseller meydana
getirir ve yüzey aktif madde adlandırılır
(Şekil 1.2.G.1.1). Sulu sistemlerdeki misel oluşum termodinamiklerinin
gösterdiğine göre
|
|
|
Şekil 1.2.G.1.1: Polar bir uç ve
apolar bir uca sahip stearik asidin sembolik gösterimi. |
emülgatörün molü başına H 1-2 KJ kadardır.
Entropi değişimi ise oda sıcaklığında 140 J K-1mol-1
kadardır. Entropi değişimi pozitif olması şaşırtıcı görülsede çözgenden entropi
aktarımı söz konusu olmalıdır ve çözünen molekülleri biraraya gelir gelmez daha
rahat hareket etmeye başlarlar. Sabunun tümü, misellerin ya da sabun
moleküllerine özgü agregatların oluşumuna neden olur. Fiziksel olarak
misellerin oluşması için gerekli olan sebep sabun molekülerinin hidrokarbon
kısımları arasındaki çekim kuvvetlerinde (van der Waals) yatmaktadır. Bu
kuvvetler, elbette Şekil 1.2.G.1.2 de gösterildiği gibi moleküller birbirlerine
parelel olarak yönlendiklerinde en güçlü duruma gelir. Buna karşın, bir miselin
büyüklüğü iyonlaşmış durumdaki karboksilat grupları arasındaki elektrostatik
itme kuvvetleriyle sınırlı olduğundan miseller yalnızca yaklaşık olarak 50-100
sabun molekülü içerir. Şekil 1.2.G.1.2 de gösterildiği gibi herbir misel
hidrokarbon grupları arka arkaya ve sulu fazın dışına karboksilat grupları
gelmek üzere sabun molekülleri iki ya da çit şeklinde tabakalar içerir. Suya
yönelen kısım hidrofiliktir fakat çit şeklindeki hidrokarbonlar arasında
tabakalar güçlü şekilde hidrofobiktir.
|
|
|
Şekil
1.2.G.1.2: 0.63 N potasyum laurat çözeltisine etil benzen
katılmasıyla laminer misellerin ve küresel modele etkisi |
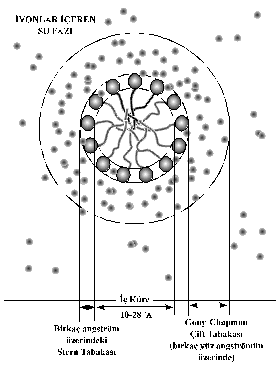
Şekil 1.2.G.1.2 de gösterilmiş olan iyonik küresel
misellerin, elektriksel doğası, daha ayrıntılı olarak iki boyutlu gösterimi
Şekil 1.2.G.1.3 de verilmiştir. Bu tip misellerin ortalama yarıçapı 12-30 °A dır. Yukarıda da
söylendiği gibi agregatın hidrofobik kısmı sıvı parafine benzer yapısı ile
miselin iç küresini oluştururken, polar baş kısımlar misel su arayüzeyine
sabitlenmiş şekildedir ve su moleküllerinin bir kısmı ile hidrate olmuş
durumdadır. Su moleküllerinin bir kısmı ise misel tarafından tutulmuştur. Yüklü
baş kısımlar ve iyonik misellerin küçük zıt iyonlar belli bir bölgede
yoğunlaşmış olup misellerin bittiği yüzey dışındaki birkaç angströmluk kısım stern tabakası olarak bilinir. Stern
tabakasının yoğunluğu misel üzerindeki net yükün azalması ile ilişkilidir. Zıt
iyonların pek çoğu bununla beraber, Gouy-Chapman elektriksel çift tabakasında
yer alırlar ve bu iyonlar yüklü agregatların iyonlaşmasıyla oluşur ve
çözeltideki iyonlarla yer değiştirebilir (Fendler E.J., Fendler J.H., 1970).
|
|
|
Şekil 1.2.G.1.3: Su fazındaki
misel ve etrafındaki elektriksel tabakalar |
Miseller oluşturmuş sabun çözeltisi içine sıvı monomerin ilavesi esnasında, sabunun küçük bir miktarı misellerden emülsiyon damlalarının yüzeyine geçerek burada stabilize edici ajan görevi yaparlar (Bovey et. all., 1965).
Polimerizasyon sürecinin başında; yüzey aktif maddelerin fonksiyonu, suda az miktarda çözünebilen monomerlerin çözünürlüğü etkiler bir role sahip olmasıdır (Tablo 1.2.G.1.1). Bütadien, stiren ve diğer pekçok monomerin sudaki çözünürlüğü ve monomer tabakasından su tabakasında çözünme hızı öylesine küçüktür ki yüzey aktif maddelerin yokluğunda, uygun bir polimerizasyon hızı verebilecek monomer su fazında bulunmaz. yüzey aktif madde, serbest radikallerle başlatılmış polimerizasyonda, su fazındaki reaksiyonun ilerlemesi için bir monomer haznesi görevi yaparlar.
|
Tablo
1.2.G.1.1: Su ve potasyum palmitat çözeltisinde
Stirenin çözünürlüðü |
||
|
Sıcaklık
/ C |
Suda
/ mol /L |
0.093
M K Palmitat /mol/ L |
|
25 |
0.00261 |
----- |
|
40 |
0.00308 |
0.096 |
|
50 |
0.00368 |
0.139 |
Polimerizasyonun başlama hızı ve
polimer parçacıklarının sayısı üzerine yüzey aktif maddelerin etkisinin
görülebileceği beklenir. Serbest yüzey aktif konsantrasyonu, polimer üzerinde
adsorbe olmaları yüzünden, polimerizasyonun ilk aşamalarında hızla azalır. Bu adımda yüzey aktif madde
tam olarak polimer parçacığı yüzeyine adsorbe olmuş durumdadır ve bu nedenle
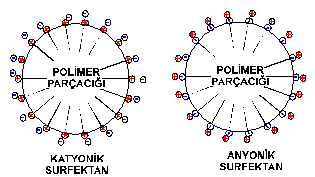
folükülasyona karşı parçacıkları koruma görevi yapmaya da başlarlar (Şekil
1.2.G.1.4). Parçacıklar, anyonik yüzey aktif maddelerin kullanılmasıyla negatif,
katyonik yüzey aktif maddelerin kullanılması ile pozitif olarak yüklenirler.
Negatif yüklü parçacıklar içeren bir lateks cam bir kabın cidarını ıslatır
fakat pozitif olarak yüklü parçacıklar negatif yüklü bir cam kabın cidarını
ıslatmaz.
|
|
|
Şekil 1.2.G.1.4: Polimer parçacığı üzerindeki emülgatörlerin
yerleşmeleri |
Folükülasyon, parçacıkların etraflarındaki çift tabakanın ortadan kalkması ile meydana gelir. Genel olarak; yüzey aktif maddenin cinsine bakılmaksızın, alkolün büyük miktarının katılması ile folükülasyon meydana gelebilir. Yağ asidi sabunlarıyla hazırlanmış lateksler asit ya da katyonların (kalsiyum, alüminyum) ilavesi ile çözünmez sabunlar şeklinde folüküle olabilirler. sülfat ve sülfonat deterjanlarla hazırlanmış negatif yüklü lateksler bir değerlikli katyonlar hariç çok değerlikli katyonlarla çöktürülebilir. Tersine, katyonik yüzey aktif maddelerle hazırlanmış lateksler bir değerlikli anyonlar hariç çok değerlikli anyonlarla çöktürülebilir.
1.2.G.2. Başlatıcı Sistemler
Ayrışma Tipi Başlatıcılar: Pekçok bileşik,
uygun şartlar altında serbest radikaller vermek üzere parçalanır. Bu parçalanma
şeklinin polimerizasyonla ilişkili olmadığına dair, ürünlerin yapılarının
belirlenmesini içeren, benzoil peroksit gibi türlerin parçalanmalarına ilişkin
kinetik analizler, hekzafeniletan gibi maddelerin çözeltilerininin magnetik
duyarlılığı gibi, pekçok kanıt vardır. Polimerizasyonu başlatma kabiliyetindeki
bu maddeler, tersinir olarak uygun şartlar altında serbest radikaller veren
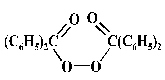
genel bir yapısal tipe sahiptirler. Bu bileşikleri tetrafenilsüksinodinitril
(I) gibi hekzasübstitüe simetrik etanları, 2-azobisizobütironitril (II), ve
potasyum persülfat (III) ve benzoil peroksit (IV) gibi anorganik ve organik
peroksi
|
(I) |
(II) |
|
(III) |
(IV) |
bileşiklerinin büyük bir kısmını kapsar. Peroksi bileşikleri oksitleyici ajanlardır ve çalışılan şartlar altında serbest radikallerin basit termal parçalanma ile mi yoksa monomer ya da sistemdeki bazı indirgeyici ajanlarla mı oluştuğunu saptamak için dikkatli deneyler gerekir. Yukarıdaki dört bileşiğin tümü simetriksel bir yapıya sahip olup bu tip bileşiklerden heteroparçalanmadan daha ziyade homoparçalanmalar beklenir (Örn. zıt yüklü iki iyondan ziyade yüksüz radikallere parçalanır). Pekçok başlatıcı diazotioeterlerde olduğu gibi simetrik değildirler.
Alifatik azo başlatıcı maddelerinden 2-azoizobütironitril, birinci mertebe bir reaksiyon ile termal olarak parçalanarak, kantitatif olarak azotun oluşumu yanısıra tetrametilsüksinodinitril verir. Eşitlik aşağıdaki şekilde yazılabilir.
|
|
(1.2.G.2.1) |
Peroksi bileşikleri,
Endüstriyel ve temel araştırmalarıda, seçkin kimyasal başlatıcılar arasında yer
alırlar. hidrojen peroksit, potasyum persülfat gibi başlatıcılar suda çözünür
özelliğe sahipken, benzoil peroksit gibi başlatıcılar yağda çözünür bir
özelliğe sahiptir. Benzoil peroksit renksiz bir katı olup çözeltisi 70-90 C ye ısıtıldığında fenil radikali oluşturan benzoil
radikali verirler.
Potasyum persülfat renksiz bir katı
olup oda sıcaklığında kuru halde tam olarak kararlı olup 20 C de 100 g suda 0.42 g potasyum persülfat çözünür fakat
tipik organik çözgenlerde çözünmezler. Sulu çözeltilerinde (bazik, nötral ya da
seyreltik asidik) stokiyometrik olarak parçalanır. Kuvvetli asitlerde ise;
|
|
(1.2.G.2.2) |
|
|
(1.2.G.2.3) (1.2.G.2.4) |
Potasyum persülfatın
katalizsiz parçalanması simetrik olarak O-O bağının parçalanmasından geçerken (a),
asit katalizli durumda simetrik olmayan bir kırılma (b) meydana gelir
|
(a) |
|
(1.2.G.2.5) |
|
(b) |
|
(1.2.G.2.6) |
Yukarıdaki bu iki parçalanma şekli organik
peroksi bileşiklerinin tipik parçalanma yoludur ( Bartlett P.D., Cotman J.D.,
1949).
Tüm
peroksi bileşiklerinde ilk adımda O-O bağı kırılırken azo bileşiklerinde N=N
bağı kalırken, iki tane C-N bağı kırılır.
Redoks Sistemli Başlatıcılar: Başlatıcılar
alanındaki göze çarpan gelişmeler, düşük ve normal sıcaklıklarda serbest
radikaller oluşturmak üzere herbiri kendi başına kararlı olan oksitleyici ve
indirgeyici ajanlar içeren, redoks sistemlerinin kullanılmasıdır.
Diazotioeterler gibi oda sıcaklığında kararsız olan ya da yüksek sıcaklıklarda
başlatıcıların termal parçalanmaları ile serbest radikallerin üretilmesine zıt
olarak, redoks başlatıcılarının teknik öneminin nedeni kararlı bileşiklerden
serbest radikallerin hızlı olarak üretilmesindendir. Bu redoks sistemlerinden
biri, hidrojen peroksit demir (II) sistemidir. Sulu çözeltide bu redoks
çiftinde serbest radikallerin oluşumu ilk olarak 1932 de Haber ve Weiss
tarafından önerilmiştir. Bu tepkime için olası bir süreç
|
|
( 1.2.G.2.7) |
|
|
(1.2.G.2.8) |
|
|
(1.2.G.2.9) |
|
|
(1.2.G.2.10) |
|
|
(1.2.G.2.11) |
şeklindedir. Yukarıdaki
reaksiyonlara göre oluşan yüksek reaktif durumdaki ![]() radikali olefinik
olmayan organik bileşiklerden (örn. metanol) bir hidrojen koparacaktır.
radikali olefinik
olmayan organik bileşiklerden (örn. metanol) bir hidrojen koparacaktır.
|
|
(1.2.G.2.12) |
Oluşan radikal demir (III) iyonlarını
indirger.
|
|
(1.2.G.2.13) |
Hidrojen
peroksit-Demir (II) demir redoks çifti ile sulu çözeltide birkaç monomerin
polimerizasyonunu başlatmada Baxendale ve grubu tarafından bildirilmiştir
(Baxendale J.H. et all., 1946). Disübstitüe bir peroksit olan persülfat,
hidrojen peroksit-demir (II) sistemine benzer bir mekanizma ile, demir (II) ile
reaksiyon verirler ve birinci adımda bir ara ürün olarak oluşan sülfat iyon
radikali
|
|
(1.2.G.2.14) |
reaksiyonuna göre
monomerle reaksiyon verir. Bu sistem için bazı adımlar aşağıda verilmiştir.
|
|
(1.2.G.2.15) |
|
|
(1.2.G.2.16) |
|
|
(1.2.G.2.17) |
|
|
(1.2.G.2.18) |
1940 da başlayan deneylerde,
Bacon R.G.R.(1946) sulu çözeltide akrilonitrilin persülfatla başlatılmış
polimerizasyonunda indirgeyici türler veren pekçok indirgeyici ajan bulmuştur.
Bunlar; pirogallol, hidrokinon ve tiyo glikolik asit gibi organik
indirgeyiciler, demir, bakır, gümüş gibi toz hale getirilmiş metaller, Cu+2,
Sn+2, Ti+2 ve Ag+ gibi bazı metal iyonları,
hidrazin ve hidroksil amin gibi azot bileşiklerini ve ![]() ,
, ![]() ,
, ![]() ,
, ![]() gibi kükürtlü
bileşiklerdir. Bunlardan başka demir (II) ile yağda çözünebilir benzoil
peroksit, kumen peroksit gibi peroksi bileşikleri kullanılabilir. Hidroperoksit
poliamin sistemleri diğer redoks başlatıcı sistemleri oluşturur. Bu sistemde,
poliamin ile demir (II) arasındaki kompleksle hidroperoksit arasında
gerçekleşir.
gibi kükürtlü
bileşiklerdir. Bunlardan başka demir (II) ile yağda çözünebilir benzoil
peroksit, kumen peroksit gibi peroksi bileşikleri kullanılabilir. Hidroperoksit
poliamin sistemleri diğer redoks başlatıcı sistemleri oluşturur. Bu sistemde,
poliamin ile demir (II) arasındaki kompleksle hidroperoksit arasında
gerçekleşir.
|
|
(1.2.G.2.19) |
Net reaksiyona göre;
serbest radikallerin oluşumu, hidroperoksit ve amin arasındaki reaksiyon
nedeniyledir. Çeşitli indirgeyici ajanlarla EDTA-demir (II) kompleksleri ile de
redoks sistemleri oluşturulabilir.
1.2.G.3.
Emülsiyon Polimerizasyonunda Parçacık
Oluşum Mekanizmaları
Polimer
parçacıklarının oluşması için önerilmiş pekçok mekanizma parçacık çekirdeğinin
oluştuğu yere göre dört ana kategoriye ayrılabilir (Vanderhoff J.W., 1985): (i)
monomerle şişmiş misellerde (Harkins V.D., 1947),(Smith W.V., Ewart R.H.,
1948), (Smith W.V.,1949); (ii) adsorbe olmuş emülgatör
tabakasında (Medvedev S.S., 1955); (iii) sulu fazda (Priest W.J.,
1952),(Jacobi B., 1952), (Fitch R.M., 1971); (iv) monomer damlalarında
(Durbin D.P. et all., 1979).
Miselli mekanizmaya (micelles mechanism) göre; başlamada, sulu
fazda üreyen radikaller monomerle şişmiş misellere girer ve polimerizasyonu
başlatır. Monomerle şişmiş polimer parçacığı oluşur. Yalnızca her 100-1000
miselden biri bir radikal yakalar ve bir polimer parçacığı oluşur. Parçacık
nükleasyon aşaması misellerin yok olmasıyla sonlanır. Monomer damlacıkları
hazne görevi yapıp, sulu fazdan diffüzyonla misellerin ve polimer
parçacıklarının monomer ihtiyacını karşılar. Monomer damlalarının içine giren
radikaller damlanın yüzey alanının göreli olarak küçük olması nedeniyle anlamlı derecede bir büyüklüğe ulaşamazlar.
Adsorplanmış-Emülgatör tabaka
mekanizmasına (absorbed-emulsifier-layer mechanism) göre; parçacık
nükleasyonu miseller, polimer parçacıkları veya emülsiyon damlalarındaki
adsorbe olmuş monomer tabakasında meydana gelir. Fikir olarak; bu mekanizma,
miseller mekanizmadaki başlamaya benzer (gerçi, eşitlikler bir dereceye kadar
farklıdır.). Sulu fazda meydana gelen ve adsorbe olmuş emülgatör tabakasına
diffüze olan bir radikal bir miselde,
polimer parçacığında veya monomer damlaları içinde muhtemelen tamamiyle eşit
olarak polimerizasyon başlar. Bununla beraber bir radikalin bunlardan birine
girme olasılığı onların nisbi yüzey alanları ile ilişkilidir. Reaksiyonun başlangıcında,
misellerin yüzey alanı emülsiyon damlalarınkinden daha büyüktür ve bu nedenle,
radikallerin monomer damlaları düşünülmeden misellere girdikleri düşünülür. İlk
oluşan polimer parçacıkları yüzey alanlarına göre radikaller için misellerle
yarışırlar. Bu nedenle, emülgatör adsorbe olmuş tabaka mekanizmasındaki
başlamada (adsorbed-emulsifier-layer mechanism) miselli mekanizmadaki (micelles
mechanism) mekanizmadaki başlama fikrindekine benzer..
Sulu faz mekanizmasındaki (aqueous phase mechanism) başlamaya göre;
sulu fazda oluşan radikallere çözünürlükleri aşılıncaya kadar monomer birimleri
katılır ve çökelir. Emülgatör adsorplamış küresel parçacıklar şeklinde oligomerik radikaller çökelirler ve monomer
adsorplamış ilk parçacıkları meydana gelir. Bu ilk parçacıklar kalırlar ya da mevcut diğer parçacıklarla
veya diğer primer parçacıklarla foluküle olurlar. Bu sistemde, emülgatörün
fonksiyonu sulu fazda çökelen parçacıkları stabilize etmesidir. Bu mekanizma
genellikle suda yeterince çözünen monomerler için uygulanır.
Nisbi olarak büyük monomer damlaları
(genel olarak 2-5m çapında) sulu fazdan radikalleri yakalamak için küçük
bir yüzey alanına sahiptirler ve bu nedenle polimerize olan oligomerik
radikaller, miseller ve polimer parçacıkları için sulu faza monomer diffüzyonu
için bir hazne görevini görürler. Olayın istatistiksel gelişmesi nedeniyle bazı
monomer damlaları radikalleri yakalar ve mikroskobik veya submikroskobik
parçacıklar şeklinde polimerize olurlar. Ana parçacık boyut dağılımından
tamamen ayrı bu parçacıkların bazıları pekçok batch polimerizasyonunda oluşur.
Emülsiyon damlalarının boyutları azaldığında monomer damlalarındaki
polimerizasyon çok anlamlı şekilde meydana gelir.
Bütün bunlardan daha farklı olmak üzere özellikle
emülgatörsüz emülsiyon polimerizasyonları için Arai ve çalışma grubu (1979)
tarafından büyüyen radikaller parçacık nükleasyonu izleyen terminasyon sonucu
ölü türleri oluşturdukları önerilirken, Vanderhoff (1967), Goodall ve çalışma
grubu (1977), Cox ve çalışma grubu (1977), Chen ve Piirma (1980), ve Vanderhoff
(1985) belli bir boyut ve konsantrasyonuna ulaşan serbest radikallerin yüzey
aktif hale geldiklerini ve miselleşmeye uğradığını kabul etmişlerdir. Ayrıca
Munro ve çalışma grubu (1979), bu mekanizmaların herhangi birinin tek başına
tüm monomerler için parçacık nükleasyonunu tanımlamasının olası olmadığını,
uygun bir şekilde göstermiştir. Mekanizmaların asıl kullanımı sudaki monomerin
çözünürlüğü üzerine iyice bağımlıdır. Homojen nükleasyon kritik misel
konsantrasyonunun altında emülgatör kullanılarak vinil asetat ve metil
metakrilat emülsiyon polimerizasyonu için Priest ve Fitch ve Tsai tarafından
önerilmiştir. Fitch ve Tsai ayrıca sulu fazda oligomerlerin polimerizasyonunun
maksimum derecesini yaklaşık 66 olarak bulmuşlardır ki metil metakrilat için
kritik zincir uzunluğu olabileceğini düşünmüşlerdir. Goodall ve Wilkinson
(1977), farklı sıcaklıklarda başlatıcı olarak ![]() ile stirenin sulu
çözeltilerinde polimerizasyonunu gerçekleştirerek, yüzey aktif oligomerlerin
miselleşmelerinin tamamen parçacık nükleasyonu ile olduğunu önermişlerdir.
Vanderhoff, Goodall ve Wilkinson emülgatörsüz emülsiyon polimerizasyonun ilk
aşamalarında elektron mikroskobu ile küçük miseller gibi parçacıkların bulunduğunu
gözlemlediklerini bildirmiştir. Bu ilk aşamalarda alınan örnekler üzerinde jel
geçirgenlik kromatografisi grafiklerinin sonuçları yaklaşık 1000 moleküler
ağırlık madde fraksiyonlarına ve 106 moleküler ağırlığından meydana
gelmiştir. Düşük molekül ağırlıklı fraksiyonun miktarı, reaksiyonun ilerlemesi
ile artma göstermemiş, yalnızca reaksiyonun ilk adımı esnasında miktarda
oluştuğu görülmüştür. Bu öneriye göre; oligomerik serbest radikaller arasındaki
terminasyonun büyük kısmı reaksiyonun ilk aşamasında meydana gelir. Tamamen
yüzey aktif oligomerlerin miselleşmeleri ile üretilen miseller,
polimerizasyonun daha ileri gitmesine yardım edip, GPC kromatograflarında
gözlenen daha yüksek moleküler ağırlıkların oluşmalarına neden olur.
ile stirenin sulu
çözeltilerinde polimerizasyonunu gerçekleştirerek, yüzey aktif oligomerlerin
miselleşmelerinin tamamen parçacık nükleasyonu ile olduğunu önermişlerdir.
Vanderhoff, Goodall ve Wilkinson emülgatörsüz emülsiyon polimerizasyonun ilk
aşamalarında elektron mikroskobu ile küçük miseller gibi parçacıkların bulunduğunu
gözlemlediklerini bildirmiştir. Bu ilk aşamalarda alınan örnekler üzerinde jel
geçirgenlik kromatografisi grafiklerinin sonuçları yaklaşık 1000 moleküler
ağırlık madde fraksiyonlarına ve 106 moleküler ağırlığından meydana
gelmiştir. Düşük molekül ağırlıklı fraksiyonun miktarı, reaksiyonun ilerlemesi
ile artma göstermemiş, yalnızca reaksiyonun ilk adımı esnasında miktarda
oluştuğu görülmüştür. Bu öneriye göre; oligomerik serbest radikaller arasındaki
terminasyonun büyük kısmı reaksiyonun ilk aşamasında meydana gelir. Tamamen
yüzey aktif oligomerlerin miselleşmeleri ile üretilen miseller,
polimerizasyonun daha ileri gitmesine yardım edip, GPC kromatograflarında
gözlenen daha yüksek moleküler ağırlıkların oluşmalarına neden olur.
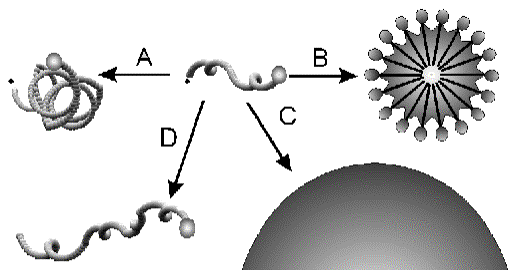
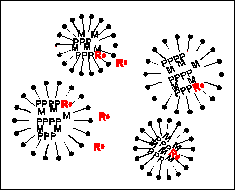
Bütün bu söylenenler ışığında özet olarak; başlatıcı ile
tepkime sonucu oluşan bir radikalin
uğrayabileceği değişiklikler aşağıda
Şekil 1.2.G.3.1 de özetlenmiştir: (A) Belli bir büyüklüğe monomerlerin
katılmasıyla büyüyen radikal, çözgende
çözünemeyeceği kritik bir zincir uzunluğuna kadar büyüdüğünde çökelir. daha
sonra çöken bu radikal emülgatörler tarafından korunurken ortamdaki
monomerlerle şişer ve polimerizasyon burada devam eder. (B) Oluşan radikal monomerle şişmiş miseller içine girerler ve
|
|
|
Şekil
1.2.G.3.1: Emülsiyon polimerizasyonunda ortamdaki bir
radikalin uğrayabileceği değişiklikler ve reaksiyon ortamında tercih
edebilecekleri yerler. |
polimerizasyon burada
ilerlemeye başlar. (C) Oluşan
radikal misellere girebildiği gibi ortamdaki monomer damlacıklarına girme şansı
da aynıdır. Fakat monomer damlacıklarının toplam yüzey alanları misellerin
toplam yüzey alanları ile karşılaştırılamayacak derecede küçüktür. (D)
Misellerin uğrayabilecekleri değişikliklerden biri de, özellikle sabun
bulunmayan bir sistemde miseller bulunmayacağı için bir kısım radikal çökelecek
kadar büyümeden ortamdaki diğer radikallerle sonlanma tepkimeleri vererek
miseller oluşturabilir. Bu dört tepkime birbiri ile yarış halindedir. Kolayca
anlaşılabileceği gibi A olayı çözgen
fazında monomer konsantrasyonu fazlayken meydana gelebilir. Çünkü, oluşan
radikal daha misellerin içine diffüzlenmeye fırsat bulamadan çökelir ve
durumdaki bir parçacığın misellerin içine diffüzlenmesinden ziyade miseller
tarafından bu radikal sarılır. Elbette bu arada misellerle birlikte monomer
molekülleri de polimer parçacığını şişirir. B olayı ise çözgen fazında monomer konsantrasyonu düşükken ortaya
çıkar çünkü A olayına tam ters bir
mantıkla oluşan radikallerin çökelecek kadar büyümeden miseller içine
diffüzlenebilecek zamanı vardır. C
olayının elbette ortamda yeteri kadar monomer bulunması şartıyla her zaman
ortaya çıkabileceğini kolayca düşünebiliriz. İhtimal dahilindeki (D) olayı ise ortamdaki radikal konsantrasyonunun
yüksek monomer konsantrasyonunun düşük olduğu emülgatörsüz sistemlerde
rastlanma ihtimali yüksek olacaktır.
Bundan
sonra incelenecek olan emülsiyon polimerizasyon sistemleri yukarıda
anlatılanlar göz önünde bulundurularak değerlendirilecektir.
1.2.G.4. Klasik Emülsiyon polimerizasyonu
Başlangıçtaki
Reaksiyon Ortamı:
Burada
monomer, alkil sülfonatlar, sabunlar ve benzeri emülsiye edici ajanlar
yardımıyla genellikle su olan bir ortamda emülsiye olurlar. Monomer, bu nedenle
emülsiye damlalar olarak hemen hemen tamamen sürekli fazda (suda) dağılırlar.
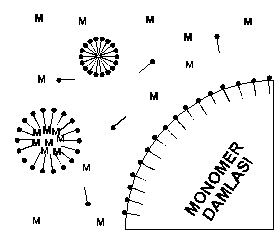
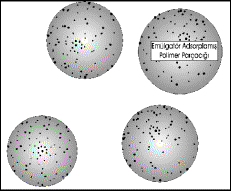
|
|
|
Şekil 1.2.G.4.1: Reaksiyon başlangıcında emülsiyon sistemi. |
Tipik bir emülgatörün su fazındaki
misel ve laminar yapısı Şekil 1.2.G.1.2 de gösterilmiştir. Bu tip oluşmuş bir
emülsiyon sistemi Şekil 1.2.G.4.1 de gösterilmiştir. Sistemde söz konusu
türler; su gibi polar bir fazda çözünmüş monomer ve miseller, misellerle
emülsiye olmuş monomer, miselleri adsorbe etmiş monomer damlalarıdır. İlk olarak polimerizasyonun emülsiye olmuş
damlaların içinde gerçekleştiği düşünülmüş ve bu nedenle emülsiyon
polimerizasyonu terimi bu tip polimerizasyon için kullanılmıştır. Gerçi şimdi
polimerizasyonda emülsiyon damlalarının ikinci derecede önemli olduklarını
bilmemize karşın bu isim yine de kullanılmaktadır.
Polimerizasyonun
Başlaması, İlerlemesi ve Sonlanması
Emülsiyon
polimerizasyonunda suda başlatıcı türlerin ortaya çıkmasıyla, suda çözünmüş
başlatıcı parçasına bağlı ilk monomerik radikaller ortaya çıkar. Emülsiyon
polimerizasyonunun girişinde de söylendiği gibi oluşan bu radikalerden bir
kısmı daha fazla büyümek suretiyle su fazındaki monomerler ile tepkimeye
girerlerken, bir kısmı da ortamdaki misellerin içine doğru diffüzlenerek büyümelerini
miseller içinde sürdürürler. Su fazında büyüyen radikallerden bir kısmı ise
kritik bir zincir uzunluğuna kadar büyüyerek çökelir. Çökelen zincirler
monomerle şişerken, bu arada ortamdaki emülgatörü adsorbe ederek
folükülasyonlara karşı direnç kazanır. Reaksiyon bu şekilde ilerlerken önce ortamdaki çözünmüş miseller kaybolur.
Daha sonra ortama monomer pompalayan monomer damlacıkları yok olur ve son
olarak miselleri oluşturan yüzey aktif maddeler yukarıda da bahsedildiği gibi
monomerle şişmiş polimer yüzeyine adsorbe olmuş şekildeki polimer taneciklerini
verirler (Şekil 1.2.G.4.2 ve Şekil 1.2.G.1.4) Reaksiyon başlarında radikallerin
sayısına göre monomer konsantrasyonunun yüksek olması ve parçacık içi
vizkozitesinin yükselmesi nedeniyle sonlanma tepkimeleri hızlı olarak
gerçekleşmez. Böylece monomerler tükenene kadar moleküller büyürler ve yüksek
moleküler ağırlıklara ulaşılır. Dönüşüm %100 civarına ulaşır. Şekil 1.2.G.4.2
de klasik emülsiyon polimerizasyonunun başlaması, ilerlemesi ve sonlanması gösterilmiştir.
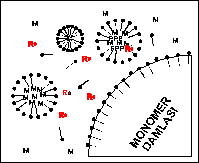
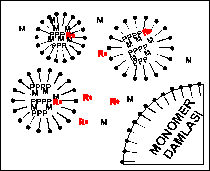
|
(A) |
(B) |
|
|
(C) |
(D) |
|
|
Şekil 1.2.G.4.1:
(A) Polimerizasyonun Başlaması (B) Polimerizasyonun sürmesi, bu
aşamada hemen tüm miseller tükenmiştir.
(C) Monomer damlaları
tükenmiş (D) Polimerizasyonun
sonlanması |
|
|
1.2.G.5.
Ters (Inverse) Emülsiyon Polimerizasyonu
Ters emülsiyon polimerizasyonu,
genelikle sulu çözeltisi halinde, suda çözünebilir bir monomerin sürekli bir
yağ fazında emülsiye edilmesi ile yapılır ve polimerizasyon yağda
submikroskobik suda şişmiş polimer parçacıkların bir dispersiyonunu vermek
üzere yağda ya da suda çözünebilir bir başlatıcı kullanılarak gerçekleştirilir
(Vanderhoff J.W., 1985). p-sodyum stiren sülfonatın ters emülsiyon
polimerizasyonunun mekanizma ve kinetikleri, yağda ve suda çözünebilir
başlatıcılar kullanılarak araştırılmıştır. Tablo 1.2.G.5.1 de bu
polimerizasyonda kullanılan bir reçete verilmiştir. p-sodyum stiren sülfonat,
suda çözünmüş ve çözelti Span 60 (sorbitan monostearat; ICI America) emülgatörü
kullanılarak o-ksilende emülsiye edilmiştir. Bazı deneylerde benzoil peroksit
o-ksilende çözünmüştür. Diğerlerinde potasyum persülfat, suda çözünmüştür. Polimerizasyonlar 40-70 C de yapılmıştır.
|
Tablo 1.2.G.5.1:
p-Sodyum stiren sülfonatın ters emülsiyon polimerizasyonu için reçete |
|
|
Bileşenler |
Ağırlık
Kesri |
|
p-Sodyum stiren sülfonat |
6.00 |
|
Deiyonize su |
24.00 |
|
o-Ksilen |
70.00 |
|
Span 60 Emülgatör |
Değişken |
|
Benzoil peroksit başlatıcısı |
0.14 |
|
Potasyum persülfat başlatıcısı |
0.060 |
1.2.G.6. Emülgatörsüz
(Emulsifier-Free) Emülsiyon Polimerizasyonu
Başlatıcı, monomer,
sürekli faz (genellikle su) ve emülgatör kullanılarak gerçekleştirilen klasik
emülsiyon polimerizasyonunda; emülgatör, oluşan ürünü kirletir. Oysa elde
edilen lateks monodispers ve temiz olursa; elektron mikroskopları, ışık
saçılma aletleri, ultrasantrifüjler ve aerosol sayma aletleri, tıbbi teşhis testleri, filtrelerin ve biyolojik zarların gözenek
çaplarının belirlenmesi gibi
uygulamalarda ve kolloid çalışmalarında model sistemler olarak çeşitli ölçme
aletleri ve tekniklerinin kalibras-yonunda geniş uygulamalarda kullanılabilecek
özellik kazanırlar (Goodall et all., 1977). Fakat emülgatörün tam olarak
uzaklaştırılması oldukça zordur ve tam olarak uzaklaştırılamaz (Van Den Hul
H.J. et all., 1971). Fakat bazı monomerler emülgatörsüz olarak da emülsiyon
polimerizasyonuna uğrayabilirler. Bu tip polimerizasyonun yürüme mekanizması
klasik emülsiyon polimerizasyonundan biraz daha farklı şekilde gerçekleşir.
Reaksiyon aşağıdaki adımlar üzerinden yürür.
1. İlk olarak sürekli fazdaki başlatıcı molekülleri ya
da iyonları (örn. ![]() ), parçalanarak (örn.
), parçalanarak (örn. ![]() ) monomerle tepkimesi sonucu yüklü radikal iyonları (örn.
) monomerle tepkimesi sonucu yüklü radikal iyonları (örn. ![]() ) verir.
) verir.
2. Daha önceki kısımlarda ele alındığı gibi; oluşan bu
radikaller bulundukları fazda yer alan çözünmüş durumdaki monomerlerle
birleşerek radikalik yüklü oligomerler
oluştururlar. Oluşan bu radikaller görünümleri açısından hidrofilik yüklü bir
uç, bu uca bağlı hidrofobik bir radikal kısmı ile, bir misel molekülünü
andırır.
Bu aşamadan sonraki aşamanın yürüyüşü,
daha önceki kısımlarda da ele alındığı gibi, ortam şartları ve reaktanların
özelliklerine bağlı olarak, birkaç olası mekanizma söz konusudur.
3. Bu oluşan misele benzer oligomerik yapının
uğrayabileceği olası değişiklikler şunlar olacaktır:
(A)- Sonlanması söz
konusu olabilir. Bu oluşan düşük molekül ağırlıklı molekül bundan sonra tam bir
emülgatör görevi yapar.
(B-1)-
Kritik
bir zincir uzunluğuna büyüyerek çökelebilir. Eğer (A) da belirtildiği gibi küçük molekül ağırlıklı misele benzer
oligomerik yapılar söz konusu değilse, çöken polimer monomerle şişer.
polimerizasyon çöken polimer fazında da ilerlemeye başlar. Polimerin
folükülasyonuna engel olacak tek kuvvet polimer molekülünün ucundaki yüklü
gruptur.
(B-2)
Bir
başka ihtimal; (A) da oluşan
emülgatörlerin miseller oluşturarak klasik emülsiyon polimerizasyondaki
mekanizmaya benzer şekilde polimerizasyonu ilerlemeye devam
ettirmeleridir.
(C) (B) kısmında oluşan tanecikler
başlangıçta yeterli yüzey yüküne sahip olmayacakları için, kolloidal olarak
kararsız parçacıklardır. Bu nedenle, onların yüzey yükleri tanecikleri
birbirlerinden uzak tutmaya yetmez ve folükülasyon meydana gelir ve kararlı
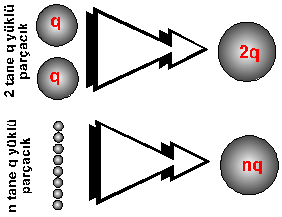
lateks parçacıklarını oluştururlar. Örneğin; İki tane q yüklü küre yeni bir
küre vermek üzere birleşirse, 2q yüklü yeni bir küre meydana gelir fakat bu
kürenin yük yoğunluğu ilk kürelerinin yoğunluğuna göre ![]() kadar daha fazladır. Eğer; n tane tanecik benzer şekilde tek
tanecik oluşturacak olursa, yeni kürenin ilk kürelere göre yük yoğunluğu
kadar daha fazladır. Eğer; n tane tanecik benzer şekilde tek
tanecik oluşturacak olursa, yeni kürenin ilk kürelere göre yük yoğunluğu ![]()
|
|
|
Şekil 1.2.G.6.1: q yüklü 2 ve n
tane q yüklü taneciğin birleşerek 2q ve nq yüklü tanecikleri oluşturmaları |
kadar fazladır. İşte
bu çarpışmalarla tanecikler kritik bir büyüklüğe ulaştıklarında üzerlerinde
kritik bir yük yoğunluğuna da sahip olurlar. Bu yükün değeri en azından,
birbirine belli bir kinetik enerji ile yaklaşan tanecikleri durdurabilecek bir
büyüklüktedir (Şekil 1.2.G.6.1). Böylece sistemdeki tanecikler birbirlerine
dokunamadıklarından kararlı bir kolloidal sistem oluştururlar. Sistemdeki bu
potansiyel engelinin büyüklüğü tanecikler üzerindeki elektriksel çift tabaka
ile ilgilidir ki bu ortamın dielektrik sabiti ile oynanarak değiştirilebilir
(Adamson A.W., 1990), (Ottewill R.W., 1977), (Midmore B.R., Hunter R.J., 1988).
(D) Tanecik içindeki
moleküllerin büyüklüğünün artması ve ortamdaki monomer damlacıklarının
tükenmesi sonucu parçacık içi radikal uçların jel etkisi nedeniyle
hareketlilikleri düşecek ve böylece polimerizasyon hızında bir artma
gözlenecektir.
4. Bundan sonra bilinen
yollarla tanecik içinde sonlanmalar meydana gelecektir.
Buradaki en önemli noktalardan biri; kolloidal taneciklerin
kararlılığını sağlayan yüklü yüzey
gruplarının başlatıcıdan doğmasıdır. Klasik emülsiyon polimerizasyonunda
kolloidin kararlılığı; başlatıcıdan
gelen yüklü gruplar + emülgatörden gelen gruplar ile sağlanırken, bu tip polimerizasyonda ancak başlatıcıdan gelen yüklü gruplar ile sağlanacaktır. Bu nedenle
taneciklerin klasik emülsiyon polimerizasyonundaki tanecik-lerle
karşılaştırıldığında bu tip polimerizasyon ile elde edilen taneciklerin daha
büyük olması beklenebilir ki bu gerçekten böyledir.
Parçacık
büyüme mekanizması iki farklı şekilde gerçekleşebilir.
İçküre-Kabuk Teorisi: Parçacık içinde monomerin
serbest radikal polimer zincirleri ile tepkime vermeleri için gerekli
şartlardan ilki, elbette, parçacık içi bu iki unsurun bir araya gelmesidir.
Ayrıca tanecik içi radikal konsantrasyonunun parçacığın her tarafına homojen
bir şekilde dağıldığını düşünürsek, polimerizasyonun tanecik içindeki her
noktada eşit şansla ilerlemesini bekleyebiliriz. Buna karşın taneciğin içinde
bulunduğu ortamı göz önünde bulundurursak, beklentimizden bazı sapmaların
olması kaçınılmazdır. Çünkü, eğer zincir uçları parçacık içine tamamen
rastlantısal olarak dağılsa bile monomer
|
|
|
Şekil
1.2.G.6.2: Polimer taneciğindeki monomer-polimer
hetorojenliği |
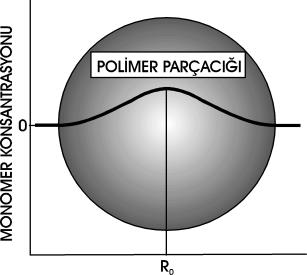
konsantrasyonu
zamanla parçacığın iç kısımlarında azalırken dış kısımlarına doğru daha fazla
olacaktır. Bunun nedenide; polimer taneciğinin iç kısımlarına ulaşamadan
monomerin zincirlerden biriyle tepkime verme şansının yüksek olmasıdır. Bu
nedenle ilerleyen reaksiyon zamanı ile birlikte parçacığın içi kısımlarında
monomer konsantrasyonu düşecektir. Bu da bizim monomerce fakir bir içküre ve
monomerce zengin bir dış kabuktan oluşan polimer taneciği gözlemlememize neden
olacaktır. Bu şekilde oluşabileceği düşünülen bir polimer taneciği Şekil
1.2.G.6.2 de sembolize olarak gösterilmiştir.
Emülsiyon polimerizasyonundaki bu tip
büyüme, genellikle, klasik emülsiyon polimerizasyonu için gözlenir.
Kabuk Büyüme Teorisi: Klasik emülsiyon
polimerizasyonundan farklı olarak emülgatörsüz emülsiyon polimerizasyonundaki
taneciklerin daha büyük olması gerektiğini daha önceki kısımlarda nedenleriyle
vurgulamıştık. Daha ileri şartları düşünmeden önce polistiren örneğini ele
alalım. Q şartları altında
polistiren için Flory eşitliğinden 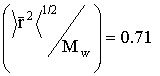 A, olarak hesaplanıp uçtan
uca uzaklık ortalaması kareleri karekökü (
A, olarak hesaplanıp uçtan
uca uzaklık ortalaması kareleri karekökü (![]() );
); ![]() =106 için 710 A ve
=106 için 710 A ve ![]() =105 için 225 A büyüklüğündedir. İlk moleküler ağırlık geleneksel olaylar
için tipikken (Smith-Ewart Olayı II), sonraki moleküler ağırlıklar emülgatörsüz
sistemlerin kabuk büyüme periyodu için tipiktir (Chen S.A. et. all., 1993). Bu
iki büyüklükten görüldüğü gibi klasik emülsiyon polimerizasyonunda moleküller
taneciğin her tarafında etkinken, emülgatörsüz emülsiyon polimerizasyonunda ise
serbest radikal uçların erişebilecekleri mesafe nisbeten daha azdır.
Emülgatörsüz emülsiyon polimerizasyon sistemlerinde kabuk-büyüme mekanizmasının
esas olarak kabuk kısmında (100-400°A) meydana geldiğini ileri sürmüşlerdir
(Chen S.A. et. all., 1993), (Chen S.A. et. all., 1990), (Chen S.A., Lee S.T.,
1990), ( Chen S.A., Lee S.T., 1991).
=105 için 225 A büyüklüğündedir. İlk moleküler ağırlık geleneksel olaylar
için tipikken (Smith-Ewart Olayı II), sonraki moleküler ağırlıklar emülgatörsüz
sistemlerin kabuk büyüme periyodu için tipiktir (Chen S.A. et. all., 1993). Bu
iki büyüklükten görüldüğü gibi klasik emülsiyon polimerizasyonunda moleküller
taneciğin her tarafında etkinken, emülgatörsüz emülsiyon polimerizasyonunda ise
serbest radikal uçların erişebilecekleri mesafe nisbeten daha azdır.
Emülgatörsüz emülsiyon polimerizasyon sistemlerinde kabuk-büyüme mekanizmasının
esas olarak kabuk kısmında (100-400°A) meydana geldiğini ileri sürmüşlerdir
(Chen S.A. et. all., 1993), (Chen S.A. et. all., 1990), (Chen S.A., Lee S.T.,
1990), ( Chen S.A., Lee S.T., 1991).
|
(a) (b) |
|
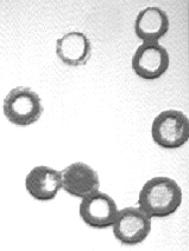
Şekil 1.2.G.6.1:
Emülgatörsüz emülsiyon polimerizasyonu ile elde edilen taneciklerin
morfolojileri (Goodall A.R. et. all., 1977) (a) TEM fotoğrafı (b) SEM
fotografı |
Kabuk büyüme mekanizmasının meydana
çıkmasının nedeni hidrofilik son grupların yüzeyde bağlanması ve parçacıkların
büyük boyutları yüzündendir (yaklaşık 0.15 - 0.20 m den daha büyük). Nitekim, Herbir büyüyen radikal
parçacık yüzeylerinde, sülfat zincir son gruplarına asılı durumda olup büyüyen
uç, uçtan uca uzaklığa eşit bir kalınlıktaki kabuk içindeki yerde olmalıdır. Bu
nedenle, kabuk bölgesinde tepkime vermeksizin taneciğin içine diffüzlenen
monomer, dışarıdaki monomerin bitmesinden sonra, taneciğin ortasında yer alan
monomer, reaktif serbest radikal polimer uçların bulunduğu parçacığın kabuk bölgesine diffüzyonu devam
eder. Böylece ise parçacık içindeki monomer konsantrasyonu düşecektir.
Polimerizasyon daha fazla ilerlediğinde monomer diffüzyonuna karşı monomer
konsantrasyonunun azalması ve parçacık içindeki vizkozitenin artması nedeniyle
bir direnç doğacaktır. Sonuç olarak polimerizasyon
|
|
|
Şekil 1.2.G.6.3: R0 yarıçaplı bir polimer taneciğinde,
su fazında monomer tükendikten sonra, parçacık içinde monomer konsantrasyonunun
değişimi. |
monomer diffüzyon kontrollü hale gelir ve
reaksiyon hızı azalır. Fick kütle transfer eşitliğine göre; verilen bir
mesafeye molekülün diffüzlenmesi için gereken zaman uzaklığın karesi ile
orantılıdır. Bundan dolayı büyük parçacıklardaki reaksiyon bölgesine,
parçacığın içindeki monomerlerin diffüzlenmesi için gereken ortalama zaman,
küçük parçacıklardakinden daha büyüktür. Sonuç olarak yüksek dönüşüm
periyodunda, monomer büyük parçacıklar
sisteminde, küçük parçacıklar sisteminden çok daha az bir hızla temin edilir.
Büyük parçacıklarda bu nedenle sınırlı dönüşüm meydana gelir.
Böylece sınırlı dönüşüm mekanizması,
kabuk büyüme polimerizasyonunun meydana gelmesine ve yüksek dönüşüm bölgesinde
monomer diffüzyon kontrollü polimerizasyonuna bağlanabilir. Bu şekilde oluşan
parçacıklardaki monomer konsantrasyonunun değişimi de verilmiştir (Şekil
1.2.G.6.4). Bu tür çalışmalar sırasında
elde edilmiş bazı parçacıkların TEM ve SEM fotoğrafları Şekil 1.2.G.6.3 de gösterilmiştir.
1.2.G.7.
Emülsiyon Polimerizasyonunun Avantaj ve Dezavantajları
Emülsiyon polimerizasyonunun bazı
avantaj ve dezavantajları açıkça görülebilir. Isı transferi hiç zor değildir.
Latekse dönüşüm sırasında emülsiyonun vizkozitesinin düşük kalması nedeniyle
ısı transferi hiç zor değildir. Süspansiyon polimerizasyonuna göre yüksek
etkili yüzey aktif ajanlar, çok hafif karıştırma ve polimer parçacıklarının
birleşme eğilimlerinin en aza inmesi nedeniyle, emülsiyon polimerizasyonu
yapışkan, kauçuksu ürünler için uygundur. Lateks ürün pek çok direkt uygulama
için uygundur. Diğer taraftan; katı polimer istenirse, çok küçük parçacıkların oldukça yüksek yüzey
alanlar nedeniyle, yüzey aktif maddelerle ve özellikle diğer suda çözünebilir
bileşenler ile kirlenmesi beklenebilir. Bu kesin olarak bir sakıncadır.
Örneğin; şekillendirmek için polistiren üretiminde berraklık istenir ya da
elektriksel yalıtım malzemeleri için polivinil klorür üretiminde sabunlar, tuzlar ya da suyun eser miktarı
dielektrik özellikleri zıt olarak etkiler.
Bir kütle ya da çözelti polimerizasyonunda (süspansiyon
polimerizasyonunun esas olarak izole olmuş damlalarda bir kütle polimerizasyonu
olduğunu hatırlayın.) ilk düşünülen, çalışılan bir sıcaklıkta büyüyen bir
polimer molekülüne belirli bir hızda monomer birimlerinin katıldığıdır. Monomerin gramı başına
polimerizasyon hızı bu nedenle büyüyen polimer moleküllerinin sayısı (örneğin
monomer başına serbest radikallerin sayısı) ile orantılıdır. Buna karşın,
sonlanma hızı büyüyen polimer moleküllerinin konsantrasyonlarının karesi ile
orantılıdır çünkü bu moleküllerin büyümesi bir diğeri ile çarpışmasıyla son
bulur. Bu nedenle, Örneğin daha aktif
bir başlatıcı ya da daha yüksek bir konsantrasyonda başlatıcı kullanılarak
serbest radikallerin konsantrasyonlarının arttırılması ile polimerizasyon
hızının arttırılması denenirse, sonlanma hızının artması nedeniyle, daha düşük
molekül ağırlıklı polimerler oluşur.
Polimerizasyon hızının başlama hızının karekökü ile orantılı olduğu ve
polimerin sayı ortalaması molekül ağırlığının başlama hızının karekökü ile ters
orantılı olduğu bulunmuştur. Polimerde monomerin çözünürlüğü yaklaşık olarak
monomerin eşit miktarı ile şişmesi ile oluşur. Serbest radikaller parçacık
içinde oluşmaz fakat, içinde başlatıcı çözünmüş su fazından parçacık içine girerler.
Serbest bir radikal bir parçacık içine girdiğinde polimerizasyon başlar ve parçacık içine diğer bir radikal girinceye
kadar devam eder. Bu nedenle, bir molekülün sonlanma olmadan önce çok
yüksek bir molekül ağırlığına büyümesi
mümkündür. Bu büyüme parçacıkların büyük bir kısmında, aynı anda ideal olarak,
parçacıkların tam yarısında sürer, çünkü aradaki suyla diğerlerinden izole
olmuşlardır ve bir parçacıktaki büyüyen bir polimer molekülü, diğer parçacık
içindeki büyüyen bir polimer molekülü ile sonlanabilir. Polimerizasyonun toplam
hızı bu nedenle yüksektir. Emülsiyon polimerizasyonunun bu özelliği (yüksek bir
hıza karşı yüksek bir moleküler ağırlığı) bu nedenle, polimerizasyonun
gerçekleştiği küçük izole parçacıkların büyük miktardaki sayısına bağlanabilir.
Parçacıkların bazı diğer tekniklerle, örneğin süspansiyon tekniği ile,
oluşturulursa bazı karakteristiklerin elde edilebileceği düşünülebilir. Bununla
beraber, şimdiye kadar süspansiyon tekniği ile gerçekleştirilen en küçük
parçacık boyutu tipik emülsiyon polimerizasyonunki ile gerçekleştirilenden,
çapı 10 kat ya da hacimlerinden 1000
kat farklıdır. Bu nedenle 0.5 lik lateks parçacıklara karşı süspansiyondaki
parçacıklar 5 olup, birim hacimdeki toplam
parçacıkların ağırlığı aynıdır. Lateksteki kadar süspansiyonda da aynı
polimerizasyon hızına ulaşmak için süspansiyondaki taneciklerin yarısı herbiri,
1000 büyüyen polimer molekülü ya da parçacıklarının tümü başına 500 büyüyen
polimer molekülü içermelidir. Her iki olayda, herbir parçacık içindeki büyüyen
moleküllerin hızlı karşılıklı sonlanması, çok düşük moleküler ağırlıklı bir
polimerin oluşmasına neden olacaktır. Radikal oluşumunun çok yüksek bir
hızı örneğin, yüksek bir başlatıcı
konsantrasyonunda ayrıca gerekli olacaktır. Süspansiyon tekniği, bu nedenle,
çok yüksek moleküller ağırlıklı polimerlerin hızlı üretilmesi için uygun
değildir. Pratikte, makul bir reaksiyon hızında, süspansiyon polimerizasyonu
ile elde edilebilir moleküler ağırlıkları pekçok uygulamalar için uygun olup
emülsiyon polimerizasyonu ile elde edilebilen moleküler ağırlıklar öylesine
yüksektir ki genellikle moleküler ağırlıklarını ayarlamak için bir değişiklik
gereklidir.
Süspansiyon ve emülsiyon polimerizasyonlarının herikisinde
de uygun dispersiyon ortamı sudur. Bu iki nedenle gereklidir. (1) pekçok monomer destilasyon ile
tekrar elde edilebilir düşük molekül ağırlıklı pekçok diğer (organik) solventte
çözünebilir. (2) su ucuz ve
tehlikesizdir. Dört bileşeni Monomer (örneğin stiren), sürekli faz (su),
emülgatör (sodyum sabunu), ve başlatıcı (potasyum persülfat) içeren emülsiyon
polimerizasyonu için basit bir reçete
Tablo 1.2.G.7.1 verilmiştir.
|
Tablo 1.2.G.7.1: Stirenin
emülsiyon polimerizasyonu için basit bir reçete |
||
|
Bileşenler |
Ağırlık oranları |
|
|
Stiren |
100 |
|
|
Su |
180 |
|
|
Sodyum sabunu* |
5.0 |
|
|
Potasyum persülfat |
0.15 |
|
Memnuniyet verici polimerizasyonu elde edebilmek için sadece bileşenlerin uygun bir kaba yüklenmesi yeterli olup, monomerden tamamen atmosferik oksijen uzaklaştırılır ve azot atmosferi oluşturulur ve sıcaklık 50C de tutulurken makul bir karıştırma ile bileşenler karıştırılır. Süspansiyon polimerizasyonuna zıt olarak, dönüşüm hızı ve parçacık boyutunu kapsayan sonuçlar, geniş sınırlar arasında karıştırma şekline az miktarda bağımlı olduğunu gösterir. Yukarıdaki reçete ile dönüşüm hızı 50 C de saatte yaklaşık % 50 iken başlatıcı miktarı gösterilenden 4 defa fazlayken hız yaklaşık olarak 2 kat büyür.