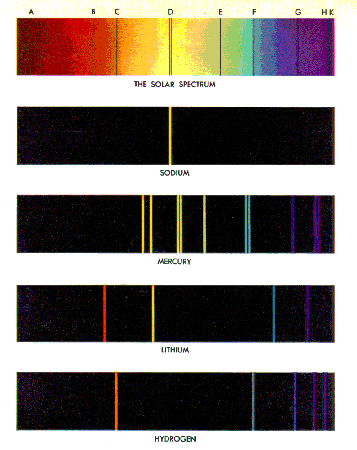
Atomik ve Moleküler SpektrumlarAtomlarýn ye da moleküllerin absorbe ettikleri veya yaydýklarý radyasyonlarýn frekanslarý gözlendiđinde enerjinin kuantize olduđuna dair direk kanýtlarý ele geçmeye baţlar. Tipik bazý atomik spektrumlar Ţekil 1'de verilmiţtir.
Bilindiđi gibi Rutherfort atom modeli tarafýndan aydýnlatýlamamýţ noktalardan biri atomik spektrumlardaki kesikli çizgilerin varlýđýydý. Bohr atom modelinde atomda elektronlarýn dolaţabildiđi belirli yörüngelerin varlýđýnýn kabulü ile birlikte bu çizgilerin nedeni de açýklandý. Bu teoriye göre; Bir elektron çekirdek etrafýnda hareket ederken çekirdek ile elektron arasýndaki Coulomb kuvvetil ile elektronun sahip olduđu merkezcil kuvvetin birbirine eţit olmasý gerekir. Aksi durumda elektron ya çekirdeđe düţmeli veya bulunduđu yöüngeden savrulup gitmelidir. Bu nedenle; \rm
F_{Coulomb}=F_{Merkezcil}
\qquad \qquad (Eţitlik \; 1 )
olmalýdýr. Çekirdek ile elektron arasýndaki Coulomb kuvvetinin büyüklüđü; \rm
F_{Coulomb}={ z q_e^2 \over 4 \pi \epsilon _o r^2}
\qquad \qquad (Eţitlik \; 2 )
ve merkezcil kuvvet büyüklüđü \rm
F_{Merkezcil} = { m \upsilon ^2 \over r}
\qquad \qquad (Eţitlik \; 3 )
dir. Burada, z; çekirdek yükü (proton sayýsý), \rm q_e; elektronun yükü, \rm \epsilon _o ; boţluđun elektriksel geçirgenlik katsayýsý, r; elektronun yörünge yarýçapý, m; elektronun kütlesi ve \rm \upsilon ; elektronun hýzýdýr. Bu iki hýz eţitlenirse; \rm
{ z q_e^2 \over 4 \pi \epsilon _o r^2} = { m \upsilon ^2 \over r}
\qquad \qquad (Eţitlik \; 4 )
Yörüngedeki elektronun hýzý ile ilgili; \rm
\upsilon ^2 = { z q_e^2 \over 4 \pi \epsilon _o mr} \qquad \Rightarrow \qquad \upsilon = \sqrt{ { z q_e^2 \over 4 \pi \epsilon _o mr}}
\qquad \qquad (Eţitlik \; 5 )
veya yörüngenin yarýçapý için; \rm
r = { z q_e^2 \over 4 \pi \epsilon _o m \upsilon ^2 }
\qquad \qquad (Eţitlik \; 6 )
Bu yörüngede dönen elektronun toplam enerjisi kinetik ve potasiyel enerjiden oluţacađýndan; \rm
E=E_{toplam}=E_{kinetik}+E_{potansiyel}
\qquad \qquad (Eţitlik \; 7 )
\rm
E={1 \over 2} m \upsilon ^2 + (- { zq_e^2 \over 4 \pi \epsilon _o r} )
\qquad \qquad (Eţitlik \; 8 )
Eţitlik 5 e göre \rm m \upsilon ^2 = { z q_e^2 \over 4 \pi \epsilon _o r} olacađýnda, Eţitlik 8; \rm
E={1 \over 2} { z q_e^2 \over 4 \pi \epsilon _o r} - { zq_e^2 \over 4 \pi \epsilon _o r}
\qquad \qquad (Eţitlik \; 9 )
\rm
E= -{ z q_e^2 \over 8 \pi \epsilon _o r}
\qquad \qquad (Eţitlik \; 10 )
ţeklinde yeniden düzenlenebilir. Bohr tarafýndan öne sürülen ţart elektronun açýsal momentumunun \rm h/2 \pi 'nin tam katlarý olmasý gerekiyordu. Yani; \rm L= m \upsilon r = { nh \over 2 \pi } \qquad \Rightarrow \qquad L= m \upsilon r = { n \; \hbar } \qquad ( n = 1,2,3, ...).
\qquad \qquad (Eţitlik \; 11 )
Buna göre elektronun hýzý \rm \upsilon için; \rm
\upsilon = { n \hbar \over m r }
\qquad \qquad (Eţitlik \; 12 )
yazýlabilir. Eţitlik 5 de bu hýz büyüklüđü yerine konursa \rm
\upsilon ^2 = { n^2 \hbar ^2 \over m^2 r^2 } = { z q_e^2 \over 4 \pi \epsilon _o mr}
\qquad \qquad (Eţitlik \; 13 )
Böylece yörünge yarýçapý; \rm
r= { 4 \pi \epsilon _o \hbar ^2 \over m q_e^2} { n^2\over z}
\qquad \qquad (Eţitlik \; 14 )
olarak elde edilebilir. Bu denklem bize hidrojen atomuna benzer tek elektronlu atomlarýn Bohr yarýçapýný verir. r deđeri toplam enerji denklemi olan Eţitlik 10 da yerine konulursa; \rm
E=-{ z^2 q_e^4 m \over 8 \epsilon _o h^2 } {1 \over n^2}
\qquad \qquad (Eţitlik \; 15 )
ifadesi elde edilebilir. Ýki enerji seviyesi arasýndaki fark \rm
\Delta E = { z^2 m q_e^4 \over 8 \epsilon _o ^2 h^2} \Big( { 1 \over n_2 ^2 } - { 1 \over n_1 ^2 } \Big)
\qquad \qquad (Eţitlik \; 16 )
ţeklinde bulunabilir. Ayrýca \rm E= h \nu veya E= \rm {h c \over \lambda } olduđundan; \rm
{ 1 \over \lambda } = { z^2 m q_e^4 \over 8 \epsilon _o ^2 ch^3} \Big( { 1 \over n_1 ^2 } - { 1 \over n_2 ^2 } \Big)
\qquad \qquad R= { m q_e^4 \over 8 \epsilon _o ^2 ch^3}=1.097 \times 10^7 \; m^{-1}
\qquad \qquad \qquad (Eţitlik \;2)
bađýntýlarý ile verilmiţtir ( Örnek ). R; Rydberg sabiti olarak adlandýrýlýr. de Broglie dalga bađýntýsý kullanýldýđýnda Bohr modelindeki açýsal momentumun \rm h/2 \pi olma ţartýnýn nedeni kolayca anlaţýlýr.
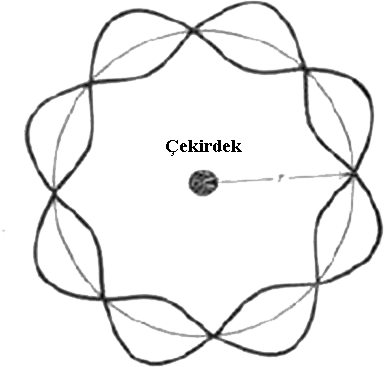
Elektronun belirli bir yörüngede kalabilmesi için yaptýđý dalga hareketinin dalga boyunun tam katlarýnýn yörüngenin çevresine eţit olmasý gerekir. Eđer yörünge tam sayýda dalga içermezse dalgalar birbirlerini yok ederler (Ţekil 2). Böyle bir sonuç ise ancak elektronun yörüngede bulunmamasý ve elektronun yok olmasý anlamýna gelir. Bu açýklamalara göre; \rm n \lambda = 2 \pi r
\rm n { h \over m \upsilon } = 2 \pi r
\rm m \upsilon r = { nh \over 2 \pi } = n \; \hbar
eţitliđi elde edilebilir ki bu Bohr'un açýsal momentum ţartý ile aynýdýr. ( Örnek )
|